この本や記事で分かること
・気体の性質
・ボイルの法則、シャルルの法則、気体の状態方程式とは何か
アボガドロの法則とは何か
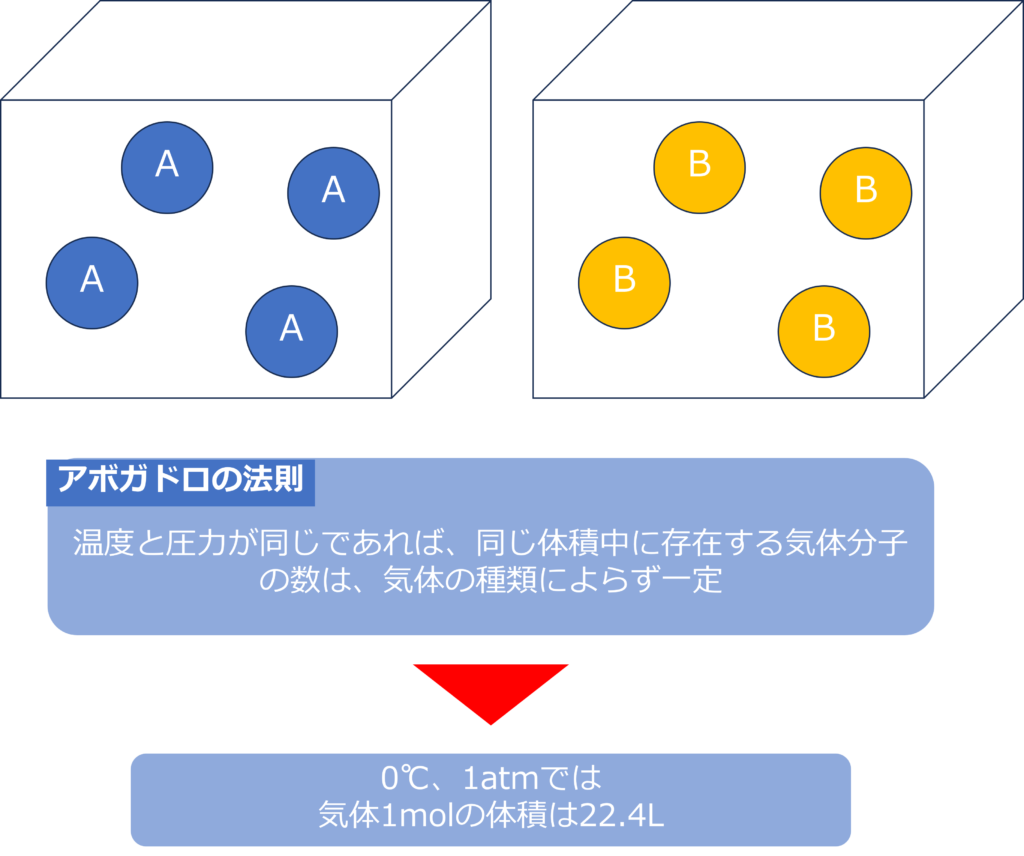
気体の体積は、温度や圧力によって変化しますが、同じ温度と圧力の場合、同じ体積中に存在する気体分子の数は気体の種類に関係なく同じになっています。
気体の種類によらず、気体分子の数が同じであることをアボガドロの法則と呼びます。
温度が0℃、圧力が1atm(1013hPa)の場合、気体1molの体積は22.4Lとなります。
圧力とはどんな力なのか
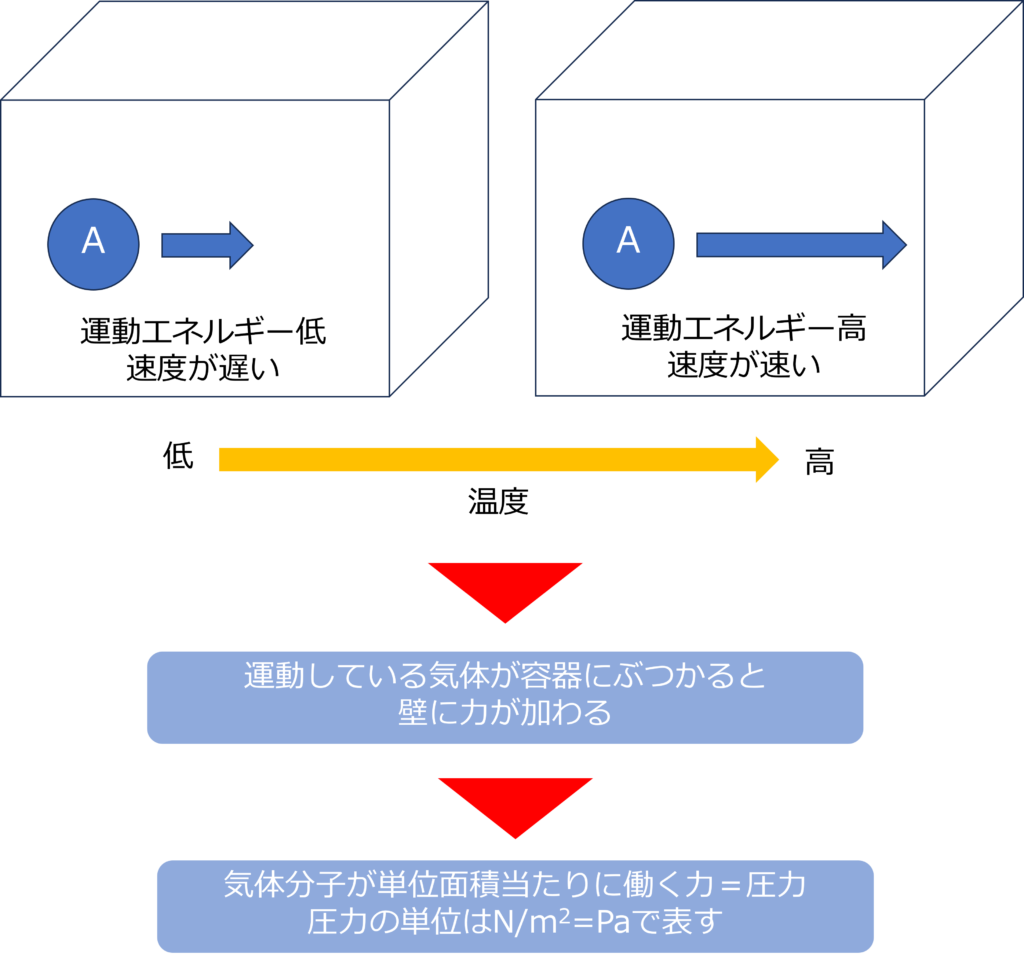
気体は多数の分子がばらばらに飛び回っており、その速度は温度が高いほど、分子の運動エネルギーが増加するため、速くなります。
運動している気体分子が容器にぶつかると、壁に力が加わります。
気体分子が単位面積(m2)当たりに働く力(N)のことを圧力といい、単位はN/m2 =Pa(パスカル)で表されます。
ボイルの法則とは何か
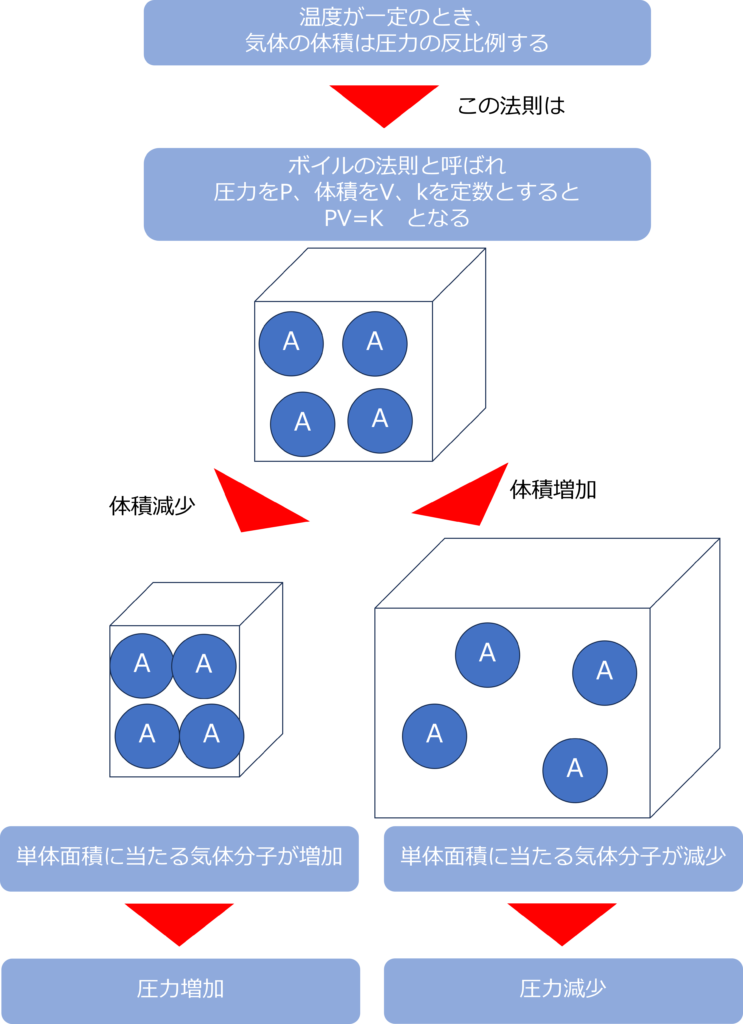
温度が一定のとき、気体の圧力と体積の間には「気体の体積Vは圧力Pに反比例する」という関係があります。
この関係はボイルの法則と呼ばれ、PV=K (Kは一定を表す定数)と表されます。
気体の体積を2倍すると、単位面積にぶつかる気体分子の数も半分になるため、衝突回数が減り、圧力が半分になります。
体積を半分にすると、気体分子の数は倍になるため、衝突回数が増え、圧力が倍になります。
シャルルの法則とは何か
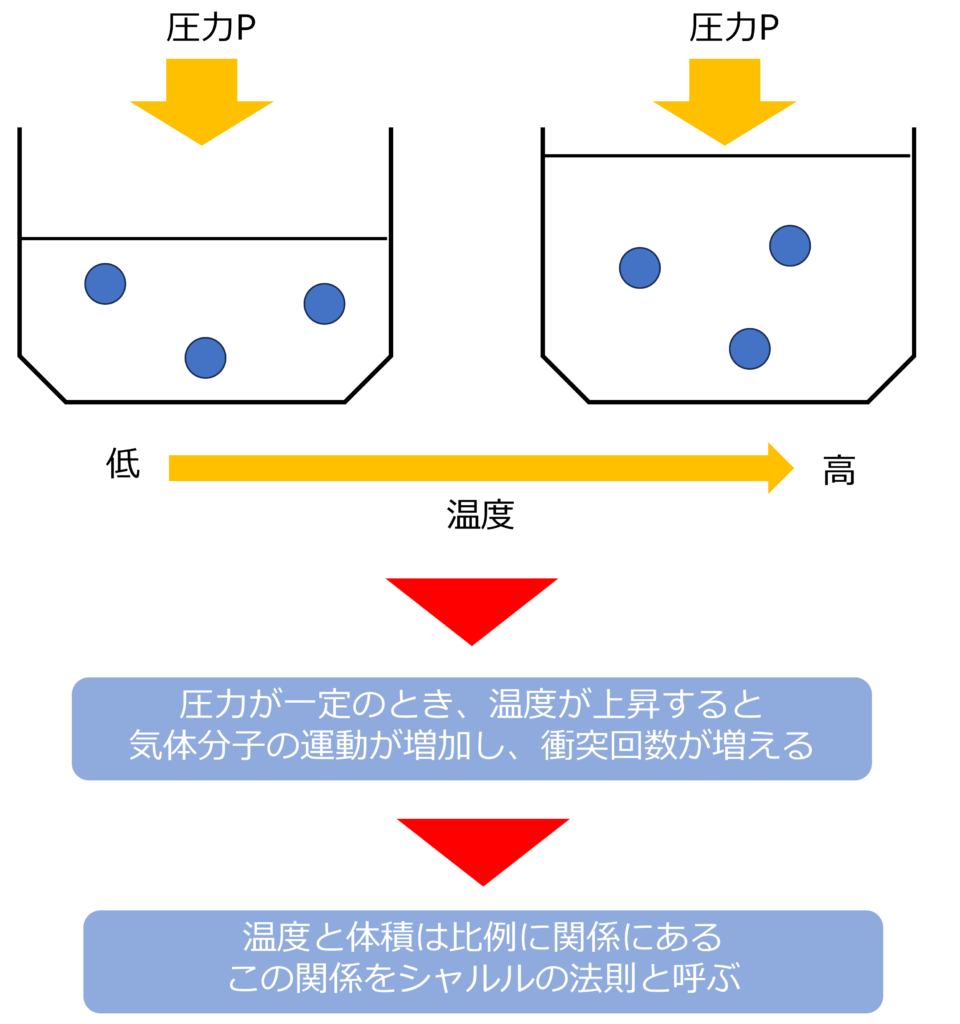
圧力が一定のときに、気体の体積と温度の間には「気体の体積Vは温度t℃が一℃上がるごとに、体積が0℃の時の体積V0の1/273づつ増加する」という関係があります。
この関係はシャルルの法則と呼ばれます。
温度が高くなると、気体分子の運動が増え、衝突回数が増えるため、圧力が一定であれば、体積が増えることになります。
分子の運動と温度にはどんな関係があるのか
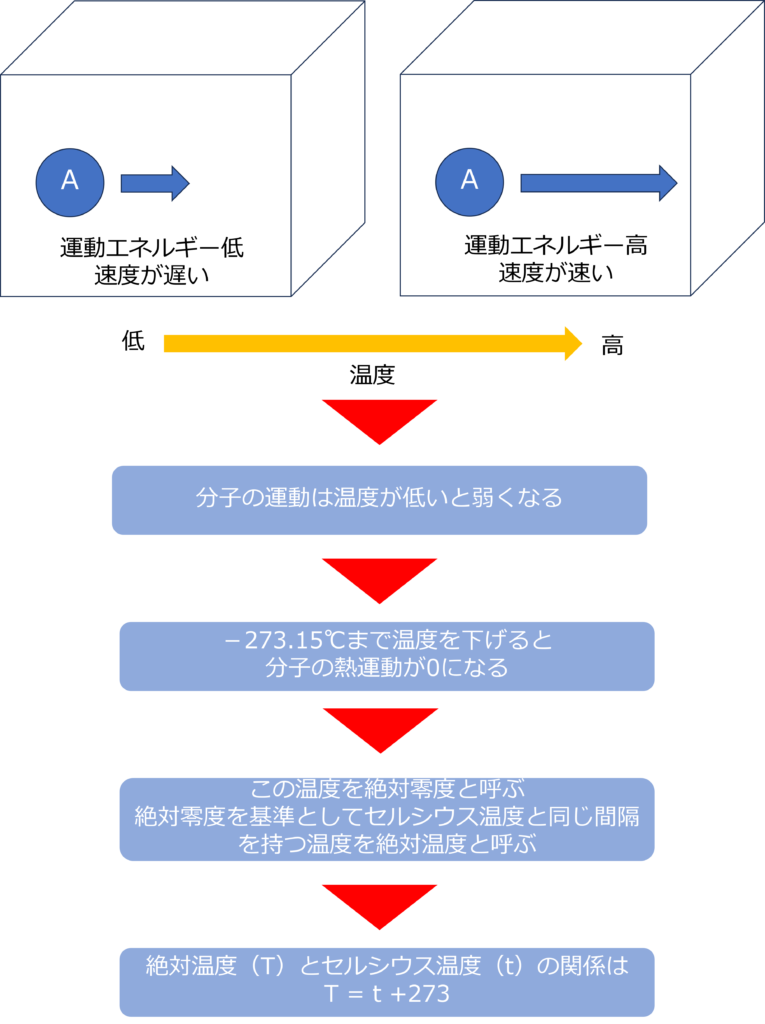
分子の運動は温度が高いほど激しく、低いほど弱くなります。
温度をどんどん下げていくと、分子の運動が低下し、‐273.℃(正確には‐273.15℃)まで下げると分子の熱運動が0になります。
この温度は絶対零度と呼ばれ、絶対零度を基準にして、セルシウス温度(℃)とおなじ間隔の目も入りで表した温度を絶対温度と呼びます。
絶対温度(T)とセルシウス温度(t)の間には、T=t + 273 の関係が成り立っています。
わずかな例外を除いて、温度は絶対零度以下になることはありませんが、上限はありません。分子が運動すれば温度は上昇し続け、何万℃、何億℃、何兆℃という温度になることもあり得ます。
ボイル・シャルルの法則とは何か
ボイルの法則とシャルルの法則は組み合わせてもなりたちます。気体の圧力をP1からP2に変化させ、体積がV1からV2に変化したとすると、ボイルの法則から、以下の式がなりたちます。
P1×V1 = P2×V2 =一定
また、同じように温度をT1からT2に変化させ、体積がV1からV2に変化したとすると、シャルルの法則から、以下の式がなりたちます。
V1/T1 = V2/T2 =一定
二つの式を合わせると、
(P1×V1 ) / T1 = (P2×V2 )/T2=一定
となり、ボイル・シャルルの法則がなりたちます。ボイル・シャルルの法則では、温度Tは絶対温度を用いて計算を行います。

気体の状態方程式とは何か
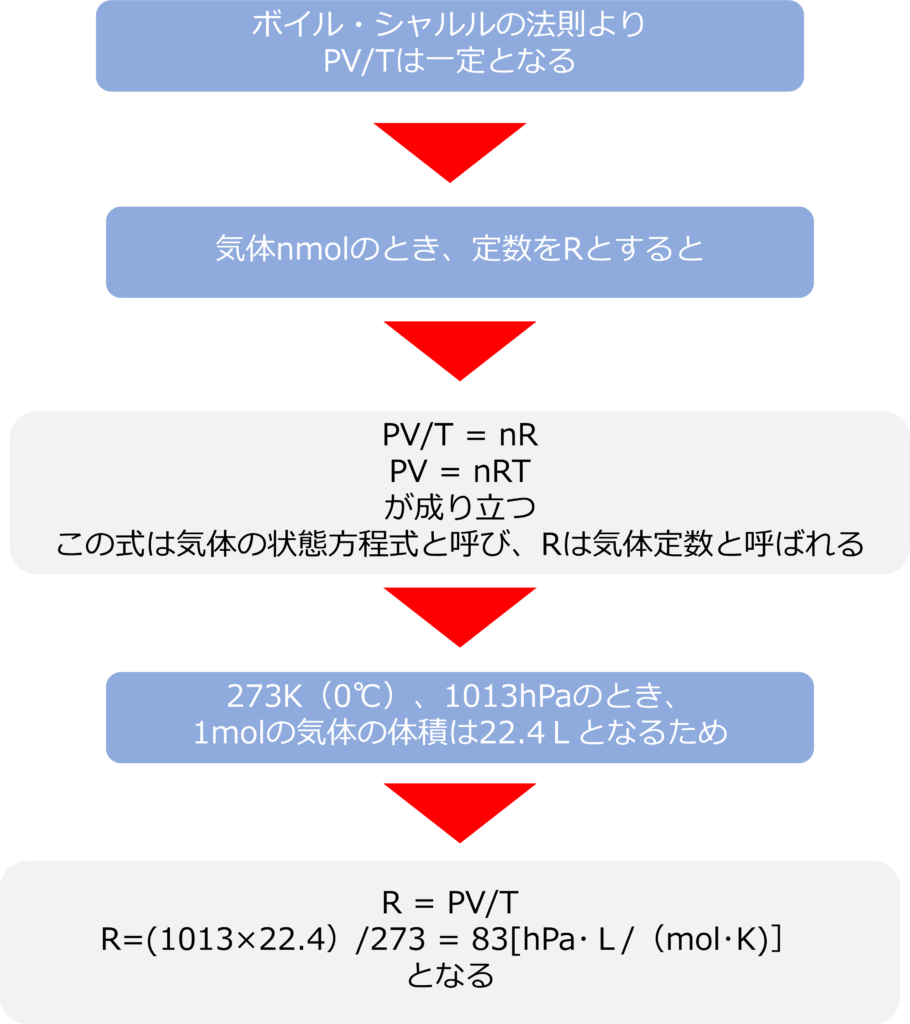
ボイル・シャルルの法則からPV/Tは一定となるため、気体1molの時、Rを定数として
PV/T=R
PV=RT
が成り立ちます。物質量をn molとすると1 mol のn倍の体積となるため
PV = nRT
が成り立ちます。この式は気体の状態方程式と呼ばれ、定数Rは気体定数と呼ばれます。
273K(0℃)、1013hPaのとき、1molの気体の体積は22.4Lとなるため、気体定数は
R = PV/T = (1013×22.4)/273 = 83[hPa・L/(mol・K)
となります。
実在気体と理想気体とは何か
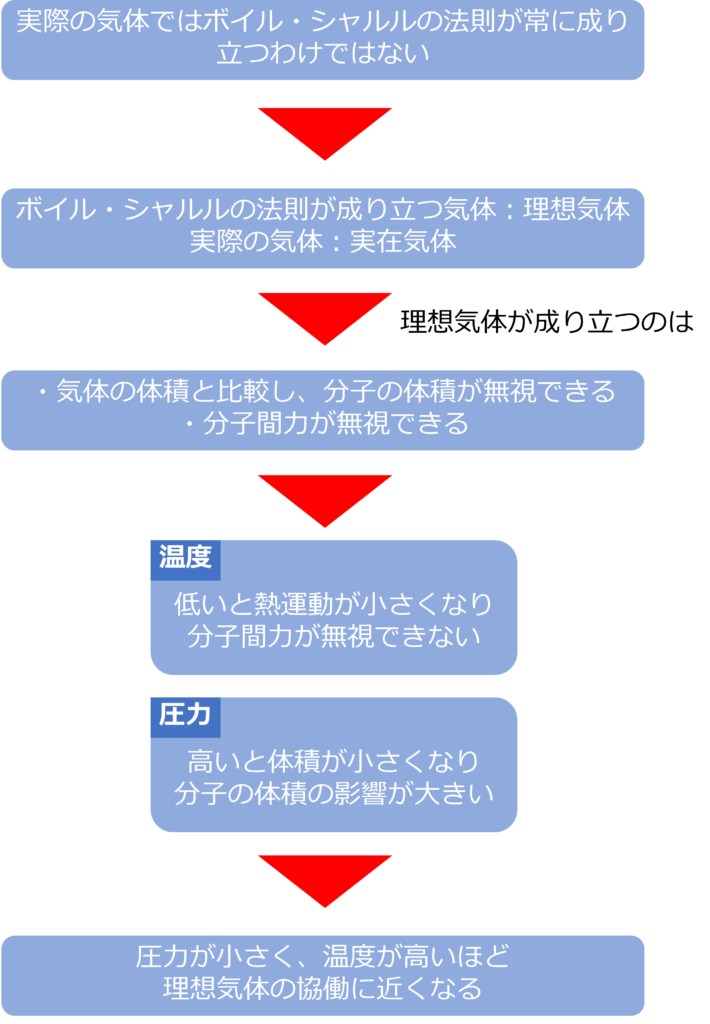
実際の気体ではボイル・シャルルの法則が常に成り立つわけではありません。
ボイル・シャルルの法則が成り立つ気体を理想気体、実際の気体を実在気体として、区別して考えるようになっています。
理想気体が成り立つには
1.気体の体積に比べて、分子の体積が無視できる
2.分子間力が無視できる
の2つが必要です。
低温になると気体の熱運動が小さくなり、分子間力が無視できなくなってきます。また、圧力が高い場合も、体積が小さくなるため気体の体積が無視できなくなっていきます。
圧力が小さく、温度が高く熱運動が激しく分子間力の影響が小さい場合には、理想気体に近い挙動をしめすようになります。


コメント