この記事で分かること
- 脱硫とは:石油・天然ガス中の硫黄化合物を除去するプロセスです。燃焼時に発生するSO₂による大気汚染・酸性雨を防ぐため、水素と触媒を使ってH₂Sとして硫黄を取り出します
- コバルトの役割:CoはMoS₂のエッジサイトに入り込み、Mo–S結合を電子的に弱めて硫黄空孔を形成しやすくします。この空孔が脱硫の活性サイトとなるため、Coは反応速度を大幅に高めるプロモーターとして機能します。
コバルト触媒による脱硫
触媒とは、それ自身は変化せずに、化学反応を促進させる物質のことです。反応に必要なエネルギーの壁(活性化エネルギー)を下げることで、通常よりも低い温度や短い時間で効率よく反応を進める役割を担っています。
現代の化学工業のプロセスの約90%に何らかの触媒が関わっていると言われているなど、私たちの生活のあらゆる場面で活躍しています。
今回はコバルトの脱硫触媒として利用に関する記事となります。
コバルトの脱硫触媒とは何か
石油精製や天然ガス処理において、硫黄化合物を除去する水素化脱硫(HDS: Hydrodesulfurization)プロセスは極めて重要です。コバルトはこのプロセスで中核的な役割を担います。
CoMo/Al₂O₃ 触媒(最も広く使用)
- 組成: CoO–MoO₃ を γ-Al₂O₃ に担持
- 活性相: Co–Mo–S 相(”CoMoS フェーズ”)
- 特徴: チオフェン類・ジベンゾチオフェン(DBT)など比較的反応しやすい硫黄化合物に高活性
- Co の役割: Mo の活性サイト(硫化物エッジ)を促進するプロモーターとして機能
NiMo との比較
| 特性 | CoMo | NiMo |
|---|---|---|
| HDS 活性 | ◎ | ○ |
| HDN(脱窒素)活性 | ○ | ◎ |
| 芳香族水素化 | △ | ◎ |
| 適した原料 | 軽質留分 | 重質留分 |
触媒の活性化メカニズム
前駆体(酸化物)→ 硫化処理(H₂S/H₂)→ 活性相(Co–Mo–S)
CoO + MoO₃/Al₂O₃ → Co-Mo-S(Type I / Type II)
Type II CoMoS が最も高い HDS 活性を示し、Al₂O₃との相互作用が弱い完全硫化型の構造です。
Coのプロモーター効果
Co原子は MoS₂ のエッジサイトに配位し:
- Mo–S 結合を弱める → 硫黄空孔(活性サイト)形成を促進
- H₂の解離吸着を助ける
- 電子的効果により硫黄化合物の吸着・活性化を改善
超深度脱硫への対応
環境規制の強化(硫黄分 10 ppm 以下)に伴い以下のような開発も進んでいます。
- バルク CoMoS 触媒(担体なし)の開発
- ナノ構造化・形態制御による活性サイト増加
- 有機添加剤(クエン酸、EDTAなど)による Type II 相の選択的生成

コバルトは単独で脱硫触媒として機能するというより、Mo の活性を最大化するプロモーターとして真価を発揮します。CoMoS という独自の複合活性相の形成が、優れた HDS 性能の鍵であり、現代の石油精製プロセスに不可欠な存在です。
脱硫とは何か
脱硫とは燃料中の硫黄化合物を除去する精製プロセスです。
なぜ必要か
硫黄化合物を含む燃料を燃やすと SO₂(二酸化硫黄) が発生し、以下の問題を引き起こします。
- 大気汚染・酸性雨 → 生態系・建築物への被害
- 触媒毒 → 自動車の排ガス触媒(三元触媒)を劣化させる
- 環境規制 → 日本・EU・米国では燃料の硫黄分を 10 ppm 以下に規制
主な脱硫方法
水素化脱硫(HDS)― 最も広く使われる
水素と触媒を使って硫黄を H₂S として除去します。
R-SH + H₂ → R-H + H₂S
(チオール) (炭化水素)(硫化水素)
除去された H₂S はさらに クラウス法 で元素硫黄(S)として回収・再利用されます。
その他の方法
| 方法 | 原理 | 特徴 |
|---|---|---|
| 酸化脱硫 | 硫黄化合物を酸化して分離 | 水素不要、軽質留分向け |
| 吸着脱硫 | 吸着剤で硫黄化合物を吸着 | 低温・低圧で可能 |
| 生物脱硫 | 微生物が硫黄を分解 | 環境負荷小、速度が遅い |
対象となる硫黄化合物
硫黄化合物の種類によって反応しやすさが大きく異なります。
除去しやすい 除去しにくい
チオール(RSH) → スルフィド(RSR) → チオフェン → ジベンゾチオフェン(DBT)
特に ジベンゾチオフェン(DBT) は芳香環に守られた構造で非常に反応しにくく、超深度脱硫の技術的な難題となっています。
工業的プロセス
石油精製所での HDS は以下の流れで行われます。
- 原料油 + H₂ を加熱(300〜400℃)
- CoMo/Al₂O₃ 触媒が充填された反応塔を通過
- 生成した H₂S をアミン吸収塔で分離
- H₂S を クラウスプラントで硫黄として回収
脱硫は石油精製の中でも特に大規模なプロセスで、世界の水素消費量の約半分が HDS に使われているとされています。

石油や天然ガスに含まれる硫黄化合物を除去するプロセスです。
硫黄化合物は燃焼すると SO₂(二酸化硫黄)になり、大気汚染・酸性雨の原因となるため、燃料として使う前に取り除く必要があります。工業的には水素(H₂)を使って硫黄を H₂S として除去する「水素化脱硫(HDS)」が主流で、CoMo/Al₂O₃ 触媒がその中心的な役割を担っています。
どのようにMoの活性化を高めているのか
MoS₂ は脱硫の触媒として以下のような欠点があります。Coによって脱硫速度を大幅に向上させることができます。
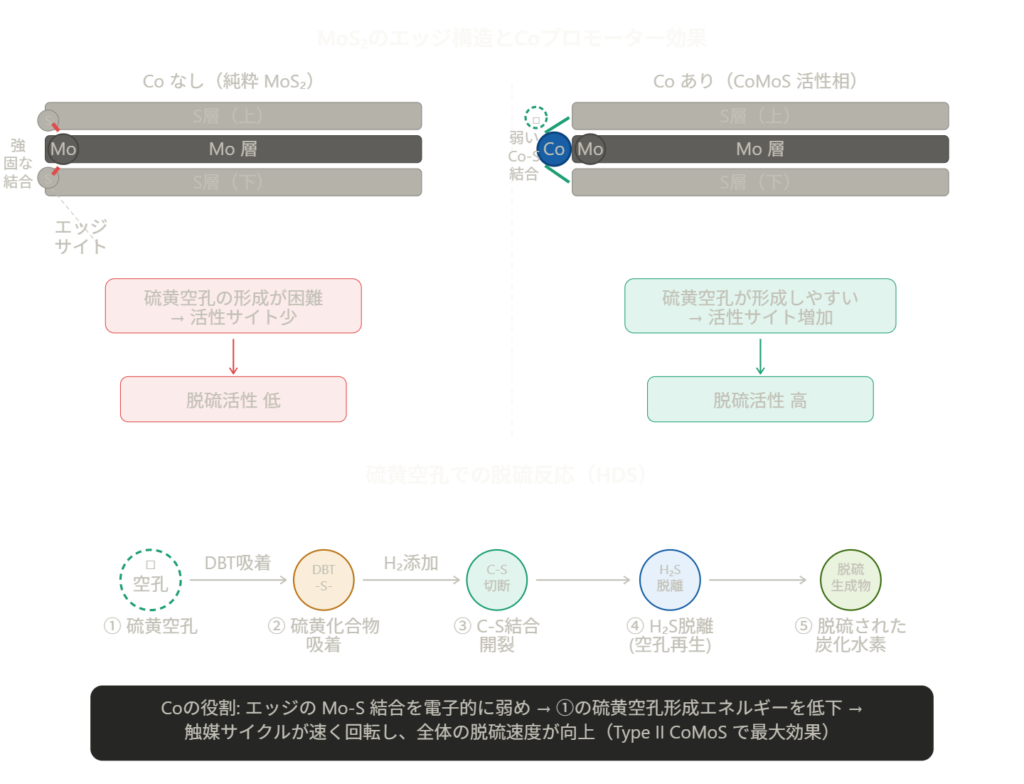
① 硫黄空孔の形成促進(最重要)
MoS₂ の活性サイトは「硫黄空孔」、つまり Mo エッジ上で S 原子が抜けた欠陥部位です。ここに硫黄化合物が吸着して脱硫反応が起こります。
純粋な MoS₂ では Mo–S 結合が非常に強く、空孔が形成されにくい。Co が Mo のエッジ位置に入り込むと:
- Co は Mo より d 電子が少なく、S との結合が弱い
- Co–S 結合の解離エネルギーが低下 → S 原子が外れやすくなる
- 結果として、H₂ による還元で空孔が形成されやすくなる
② 電子的効果(電荷移動)
Co から隣接する Mo への 電子供与が Mo の電子密度を変化させます:
- Mo の d 軌道が適度に満たされる
- 硫黄化合物(DBT など)の S 原子の孤立電子対を受け取る能力が向上
- すなわち、Mo の「求電子性活性サイト」としての機能が強化される
③ H₂ 活性化の促進
脱硫には H₂ の解離が必要ですが、CoMoS では:
- Co 上で H₂ が解離吸着しやすい
- 生じた H 原子が C–S 結合切断や H₂S 形成に効率よく使われる
Type I vs Type II CoMoS
| Type I | Type II | |
|---|---|---|
| Al₂O₃との相互作用 | 強い | 弱い(ほぼなし) |
| Co–Mo–S 完全度 | 不完全 | 完全硫化 |
| 活性 | 低 | 高い |
| 形成方法 | 通常の焼成 | 有機添加剤(クエン酸など)で制御 |
Type II が高活性な理由は、Co が Mo エッジに完全に配位でき、上記3つの効果が最大限に発揮されるためです。Coは Mo の「電子的・構造的アシスタント」として、触媒の心臓部であるエッジサイトを最適化しているわけです。

CoがMoS₂のエッジサイトに入り込み、Mo–S結合を電子的に弱めることで硫黄空孔が形成されやすくなります。この空孔が脱硫反応の活性サイトとなるため、Coは「空孔形成の促進剤」として機能し、脱硫速度を大幅に向上させます。


コメント