この本や記事で分かること
・化学反応はどのように進行するのか
・活性化エネルギーとは何か
・活性化状態では反応物はどのような構造になっているのか
化学反応はどのように進行するのか
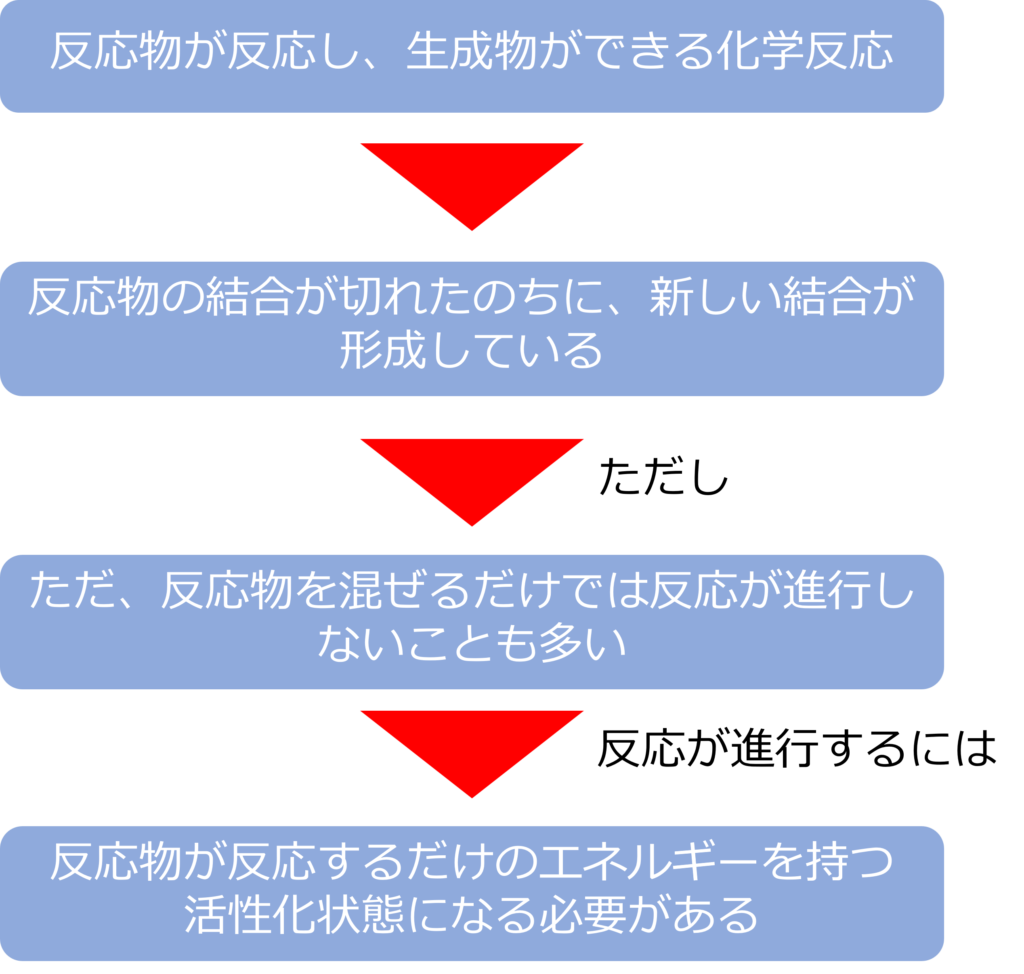
化学反応では、反応物の結合が切れ、新しい結合ができることで、生成物が生成しています。
しかし、反応物が安定である場合、ただ反応物同士を混ぜるだけでは、反応が起きることはありません。また、仮に生成物のほうが反応物よりも安定な場合でも、ただ反応物同士を混ぜるだけでは反応が進行しないこともあります。
反応が進行するには、反応物が反応できるだけのエネルギーを持つ、活性化状態になる必要があります。
外部から熱などのエネルギーを加え、反応物が反応できるだけのエネルギーを持ち活性化されたときに、化学反応は進行してきます。
活性化状態では、分子同士の結合が切れて、原子になっているのか
化学反応が進行するために必要な活性化状態になるために必要な最低限のエネルギーのことを活性化エネルギーと呼びます。
水素とヨウ素を反応させて、ヨウ化水素が生成する反応(H2+ I2 → 2HI)であれば、反応物である水素とヨウ素はそれぞれの分子で結合を生成しています。
エネルギーが加えられても、分子同士の結合が完全に切れて、原子になったのちに新しい結合ができるのではなく、活性錯体とも呼ばれる複合的な結合が形成されるため、分子同士の結合を切るエネルギーよりも活性化エネルギーは小さいエネルギーとなります。

活性化状態からどのように反応が進行するのか
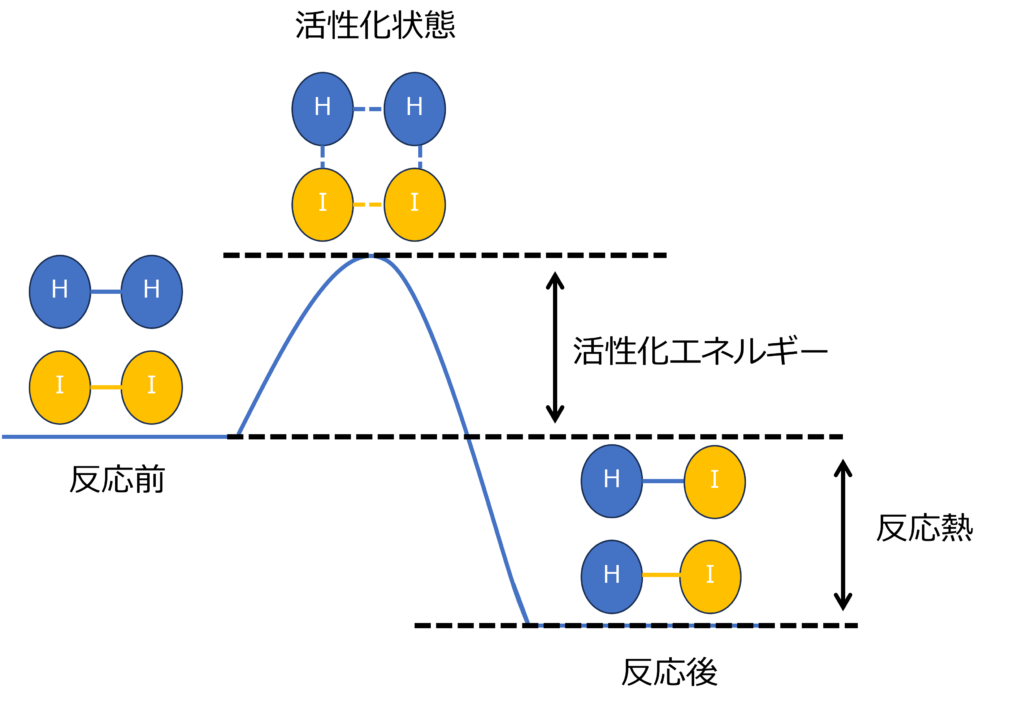
徐々にエネルギーが加えられていくと、それぞれの分子同士の結合が弱くなり、水素とヨウ素が衝突した時にH-Iの結合が生成できる状態になります。
活性化状態はとても不安定なため、エネルギーを放出し、生成物であるヨウ化水素が生成します。
生成物と反応物のもつエネルギーの差は、反応熱と呼ばれ、ヨウ化水素の場合はヨウ化水素のほうが、水素とヨウ素よりもエネルギー状態が低いため、発熱反応となります。
一方、生成物が反応物よりもエネルギー状態が高い場合は、吸熱反応となります。吸熱反応では生成物のほうが不安定な状態ではありますが、活性化エネルギーを超えるだけのエネルギーがなければ、反応物に戻ってしまうことはありません。
活性化エネルギーと反応の進みやすさはどう関係しているのか
活性化エネルギーに必要なエネルギーを持っていない粒子同士がいくら衝突しても、化学反応が進行することはありません。
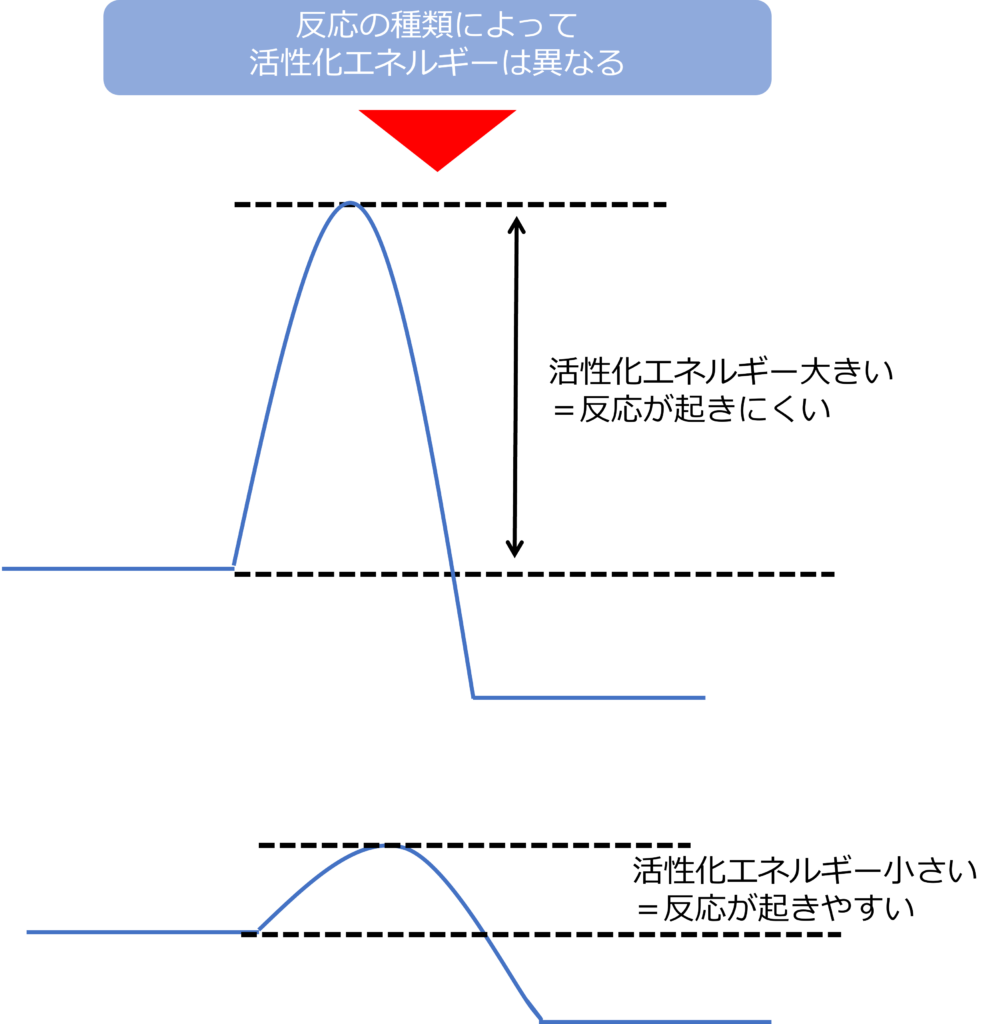
反応に必要な活性化エネルギーの涼は量はその化学反応によって異なります。
活性化エネルギーの大きい反応は外部から必要のある、熱などのエネルギーが多く必要なため、反応が起こりにくく、反応速度は遅くなります。
活性化エネルギーが小さい反応は少しのエネルギーを加えるだけで、反応が進行するため、反応が起こりやすく、反応速度も速くなります。


コメント