この本や記事で分かること
・異性体とは何か
・異性体にはどんな種類があるのか
・シストランス異性体やE,Z命名法はどんなルールで異性体を分類しているのか
異性体とは何か
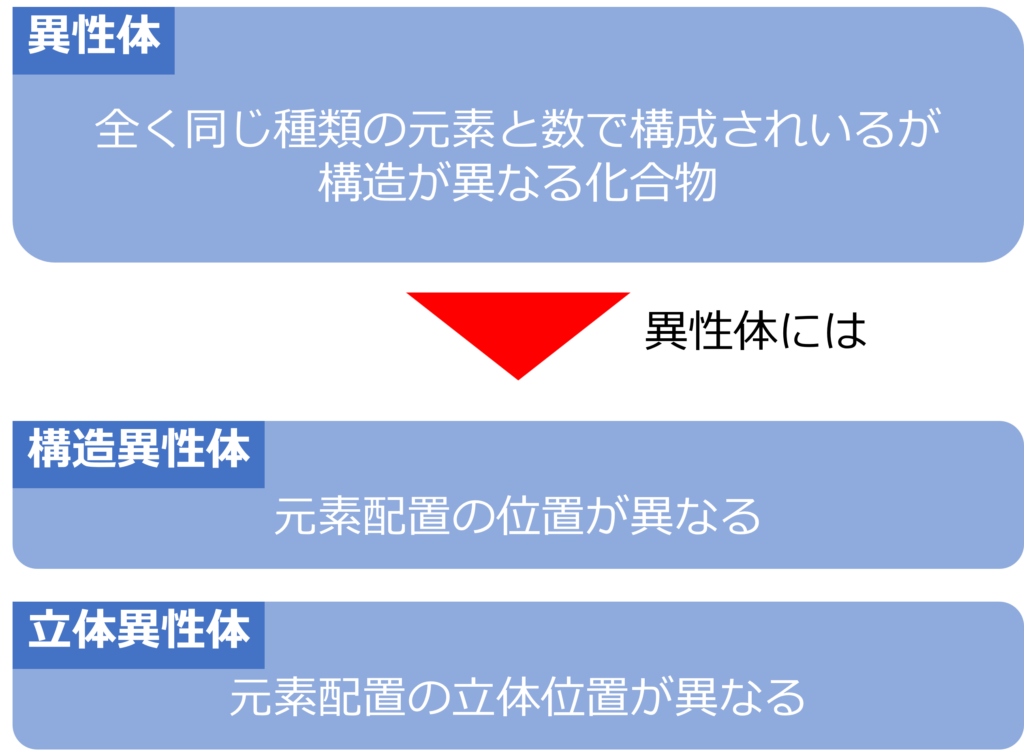
炭素を骨格とした有機化合物では、全く同じ元素の種類と数で構成されているにもかかわらず、構造が異なる物質が存在しています。
このような物質は異性体と呼ばれ、同じ構成要素でありながら、その構造の違いから性質も大きく異なっています。
主な異性体には、原子配置の位置が異なる構造異性体と立体配置が異なる立体異性体があります。
構造異性体とは何か
構造異性体にはさらに、連鎖異性体、位置基異性体、官能基異性体などがあります。
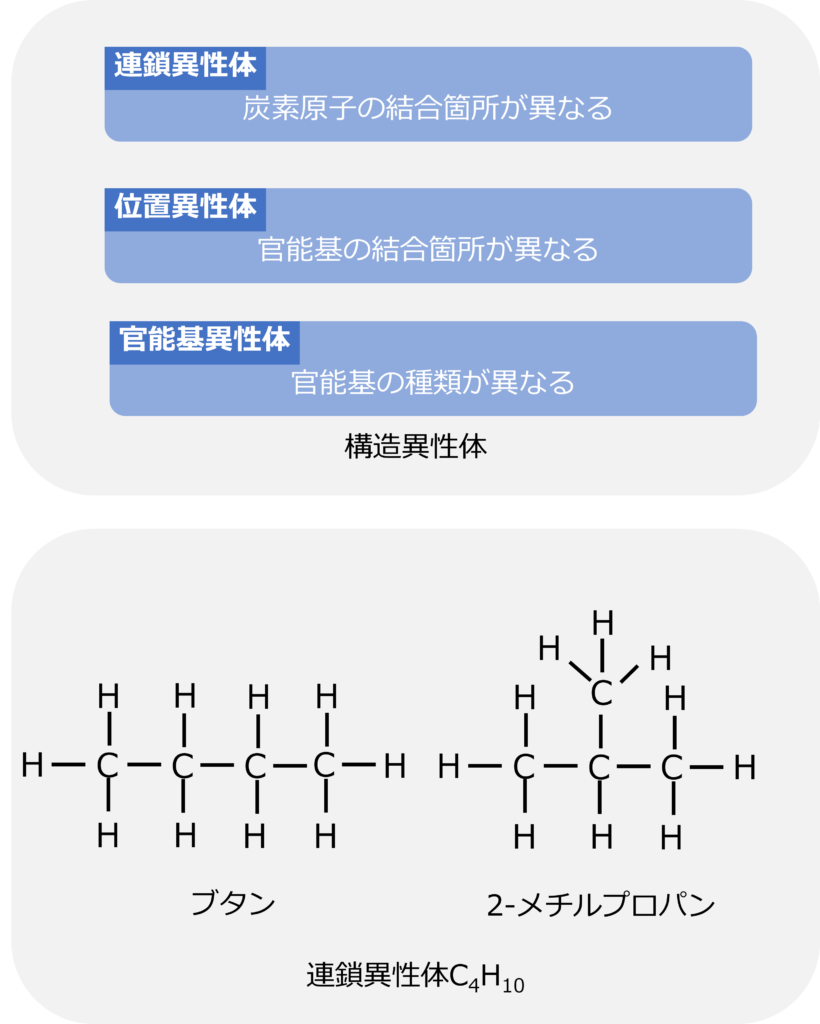
連鎖異性体は炭素原子の結合箇所が異なる異性体です。
例えば、ブタンはC4H10の化学式で表される炭化水素ですが、プロパン(C3H6)の真ん中の炭素原子にメチル基が結合した2-メチルプロパンも化学式はブタンと同じC4H10となるため、2-メチルプロパンとブタンは連鎖異性体の関係にあるといえます。
位置異性体とは何か
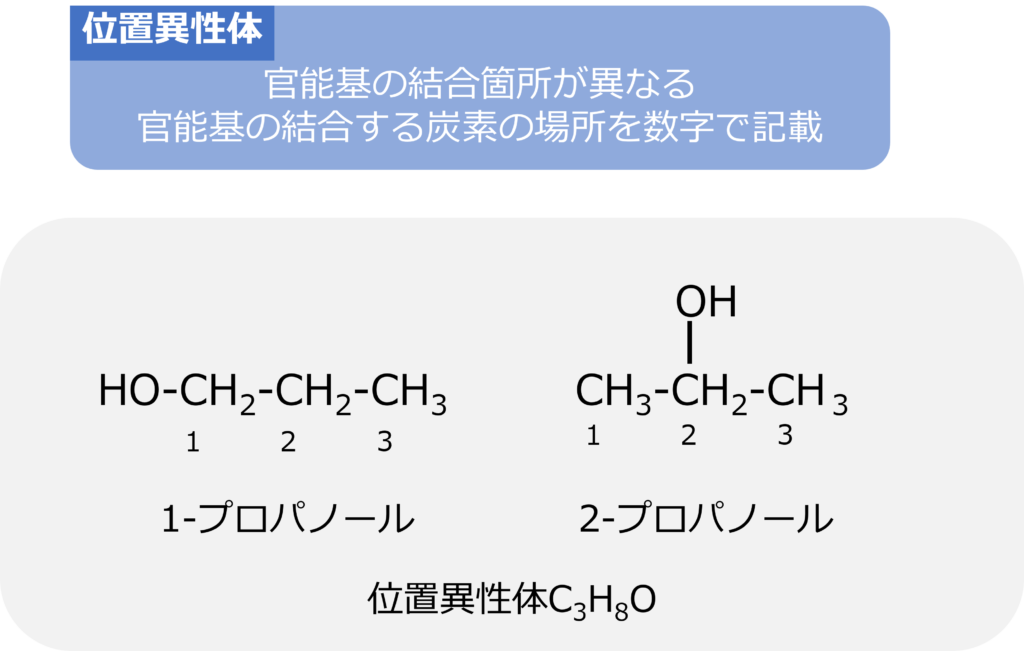
位置異性体は官能基の結合位置が異なる異性体のことです。
C3H8Oで示されるアルコールはプロパンの末端の炭素にOH基が結合したものと中央の炭素にOH基が結合したものが考えられます。
前者は1-プロパノール、後者は2-プロパノールと表し、OH基の結合する炭素の場所を数字で書くことで異性体の構造を表現することが可能です。
官能基異性体とは何か
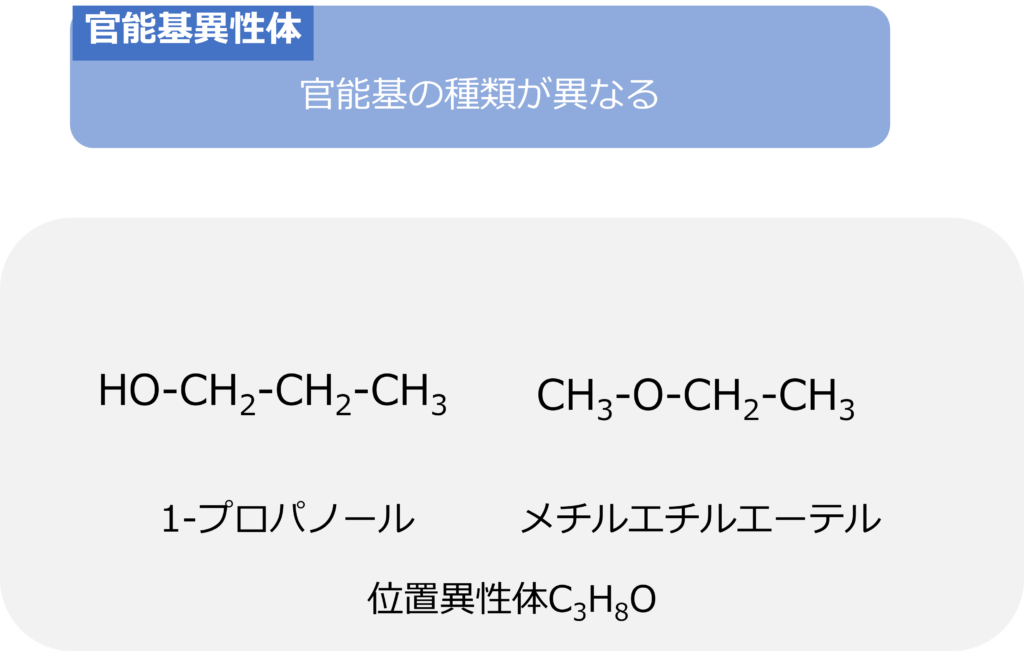
官能基異性体は原子の種類が同じでも、官能基の種類が異なる異性体のことです。
C3H8Oはプロパノールを表す化学式ですが、水酸基(OH基)ではなくエーテル結合を持つ化合物でもあります。
エーテル結合とは炭素と炭素の結合の間に酸素が存在している結合であり、C3H8Oで表される化合物の場合、メチルエチルエーテルとなり、メチルエチルエーテルとプロパノールは官能基の異性体の関係にあります。
立体異性体、シストランス異性体とは何か
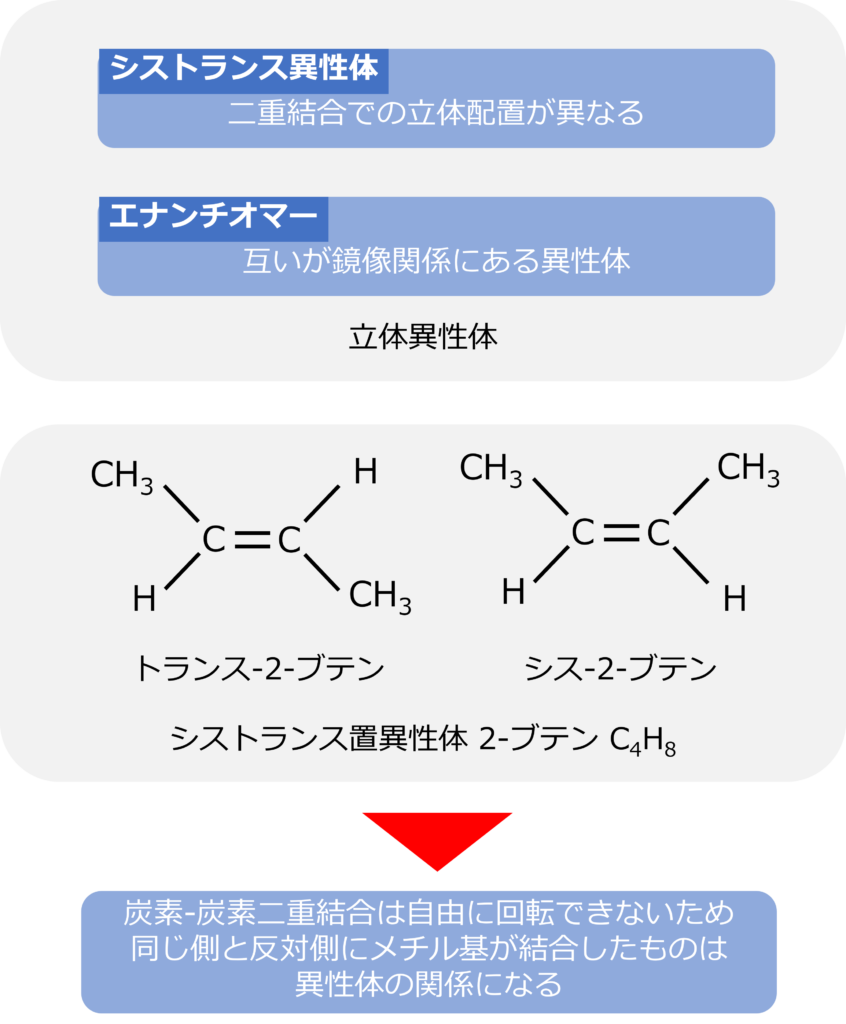
立体異性体は構成元素や官能基の結合様式は同じで、立体的な配置のみが異なる異性体のことであり、シストランス異性体(幾何異性体)とエナンチオマー(光学異性体)などがあります。
C4H8で表される化合物に炭素-炭素二重結合を持つブテンがあります。3つの炭素-炭素結合の内、中央部に二重結合がある化合物は2-ブテンと呼ばれます。
二重結合を持つ炭素にはそれぞれメチル基と水素が結合していますが、炭素-炭素二重結合は単結合と異なり、自由に回転することができません。そのためメチル基同士が同じ側に結合したものと反対側に結合したものは異なる物質として扱われます。
同じ側に結合しているものはシス(cis)、反対側に結合しているものをトランス(trans)と呼び、区別しています。
シストランス異性体で分類できないときはどのように分類をするのか
二重結合を持つ炭素に両方に水素が結合している化合物であれば、シストランスで異性体を分類することが可能です。
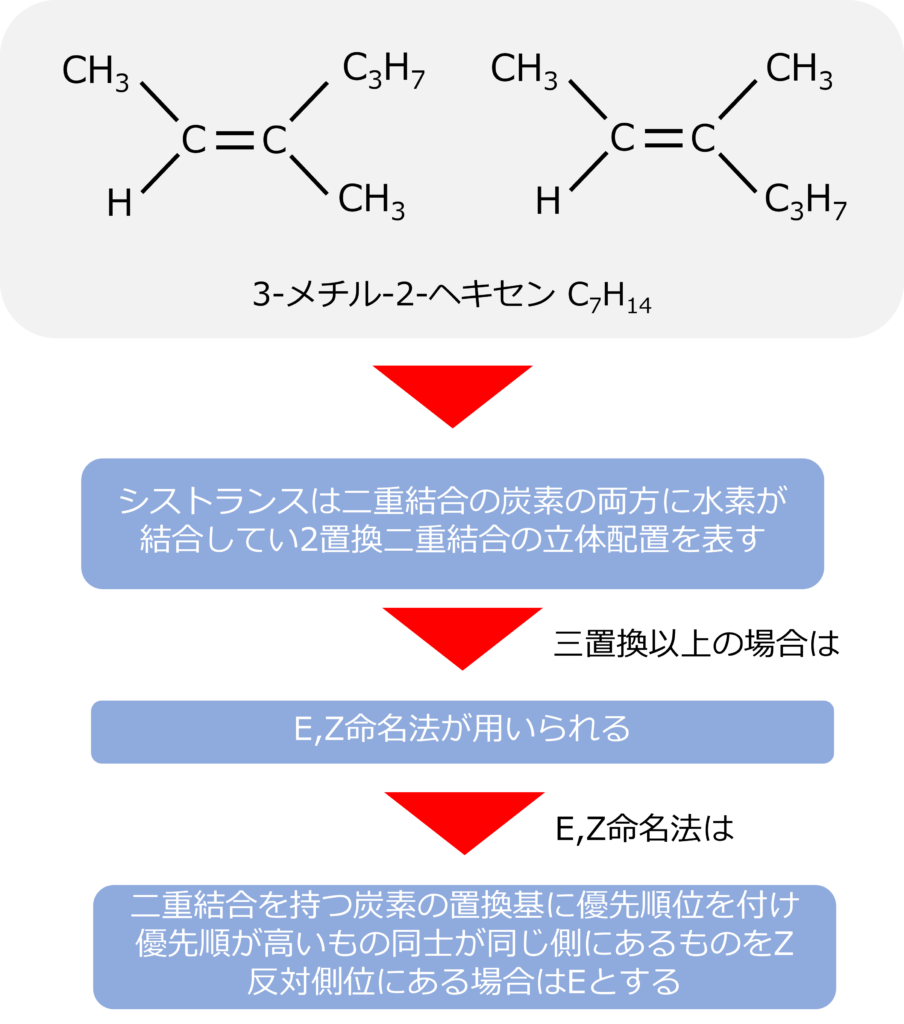
しかし、3-メチル-2-ヘキセンのような二重結合を持つ炭素の水素が他の置換基に置換されている場合、シストランスで異性体を分類することができなくなります。
このような場合はE,Z命名法が利用されます。E,Z命名法では二重結合を持つ炭素の置換基に優先順位を付け、優先順が高いもの同士が同じ側にあるものをZ(ドイツ語の一緒を表すzusammen)を、反対側位にある場合はE(ドイツ語の反対側を表すentgegen)を使用します。
E,Z命名法では置換基の優先順位をどう決めるのか
置換基の優先順位は以下のように決まります。
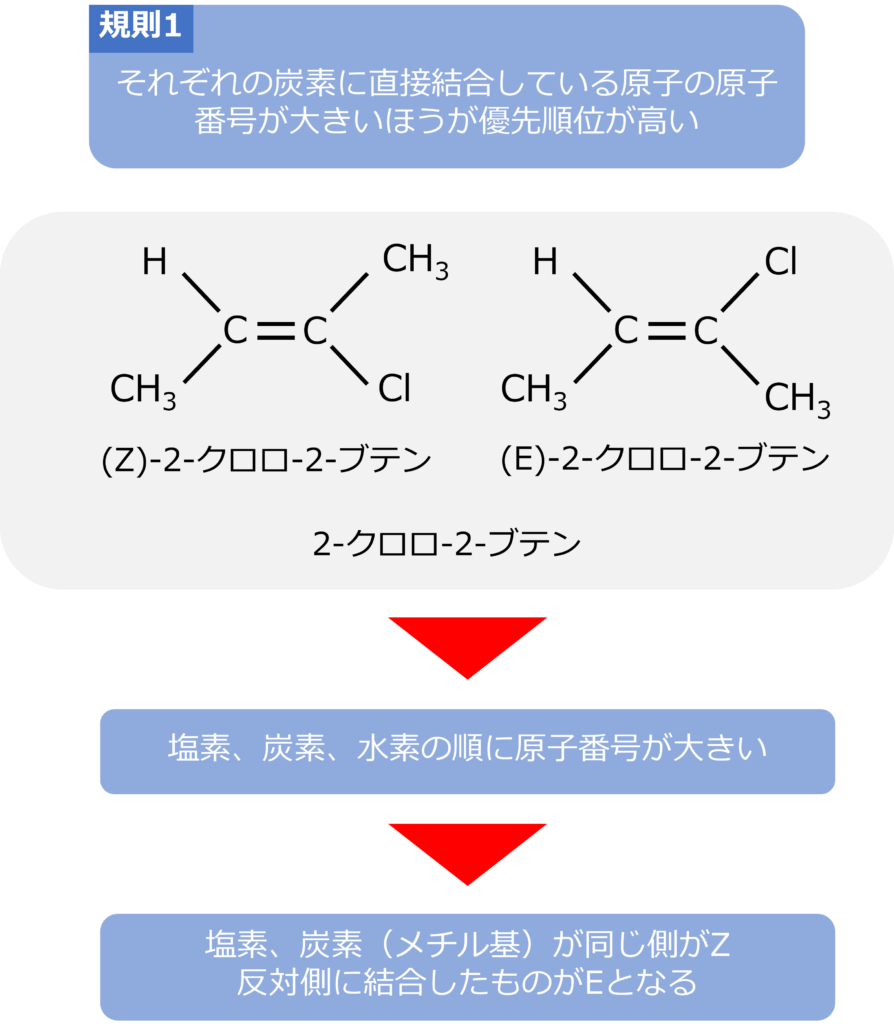
規則1 それぞれの炭素に直接結合している原子の原子番号が多いほうが優先順位が高くなる
2-クロロ-2-ブテンは二重結合を持つ片方の炭素にはメチル基と水素が、もう片方にはメチル基と塩素が結合しています。水素と炭素では炭素のほうが原子番号が大きく、炭素と塩素では塩素のほうが原子番号が大きいため、優先順位は高くなります。
そのためメチル基と塩素が同じ側にあるものが(Z)-2-クロロ-2-ブテン、反対側にあるものが、(E)-2-クロロ-2-ブテンとなります。
結合している原子が同じ場合はどうするのか
二重結合を持つ炭素にメチル基とエチル基が結合している場合、直接結合している元素は炭素となるため、規則1では優先順位を決めることができません。
そのような場合には規則の2を使用して、優先順位を付けています。
規則2 直接結合した原子同士で優先順位が決まらない場合は、二重結合を持つ炭素から2,3,4番目の元素を比較して優先順位を決める
二重結合を持つ炭素から2番目の元素は、メチル基が水素、エチル基が炭素となり、炭素のほうが原子番号が大きいため、エチル基の優先順位が高いことになります。

2番目の元素でも優先順位を決められない場合はどうするのか
置換基が二重結合を持つ場合は規則2を用いても、優先順位を決めることができない場合があります。そのような場合には規則3によって、優先順位を決定します。
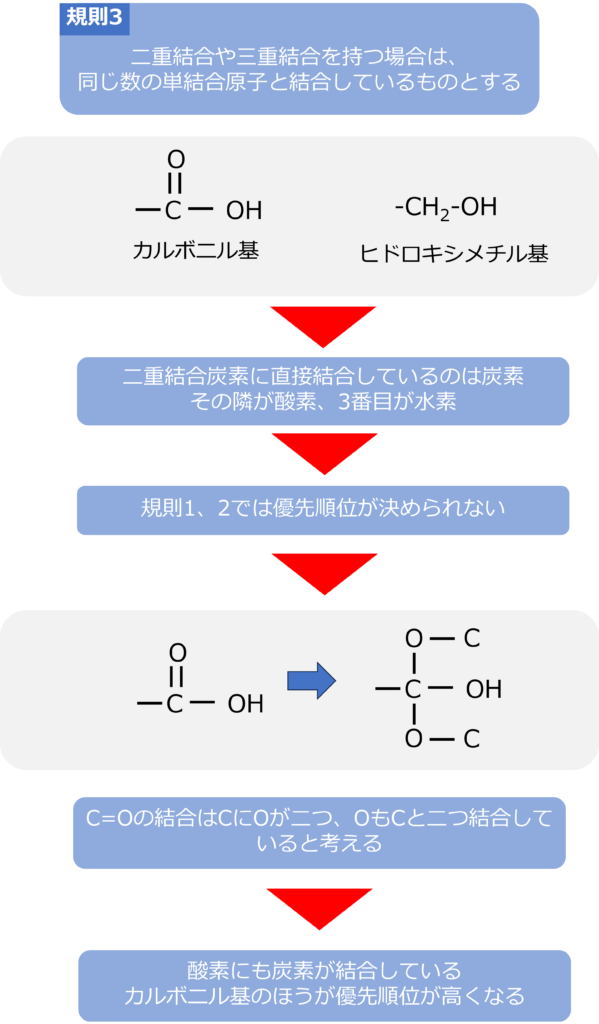
規則3 二重結合や三重結合を持つ場合は、同じ数の単結合原子と結合しているものとする
例えば、カルボニル基のような炭素と酸素が二重結合している官能基の場合、炭素は二つの酸素と結合し、酸素も二つの炭素と結合していると考えます。
カルボニル基(-COOH)とヒドロキシメチル基(-CH2OH)の場合、二重結合を持つ炭素に直接結合している原子は炭素であるため、規則1では優先順位を決めることができません。
炭素の隣の原子も酸素と水素で同じになるため規則2でも優先順位を決めることができません。
しかし、規則3により、カルボニル基は二重結合をもっているため、炭素には二つの酸素が結合し、酸素にも炭素が結合していると考えるため、カルボニル基のほうが優先順位が高いと判断することができます。


コメント