この本や記事で分かること
・反応の速度はどのように求められるのか
・反応とともに反応の速度はどう変化するか
・反応の速度を速めるためにどうすれば良いのか
反応速度とは何か
化学反応には様々な種類が存在していますが、どれくらい早く反応が進むかは反応によって様々です。
単位時間当たりの濃度変化を化学反応の反応速度と呼び、反応速度以下のように定義されています。

反応速度が速い反応ほど、反応は素早く進行します。
生成物Aから反応物Bが生成する A→Bという反応で、時刻t1におけるA、Bの濃度を[A]1、[B]1、t2での濃度を[A]2、[B]2とすると
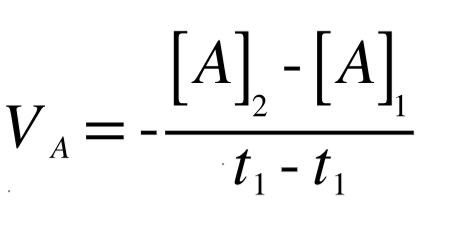
となります。また、反応速度をBの濃度変化で表すと、
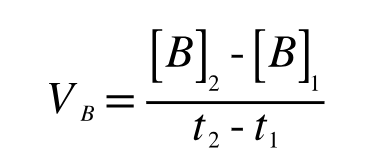
となります。速度は必ずプラスの値とする必要があります。反応物の濃度変化はマイナスの値をとるため、反応物の濃度変化から速度を算出する際には、マイナスをかけて、VAの値をプラスにする必要があります。

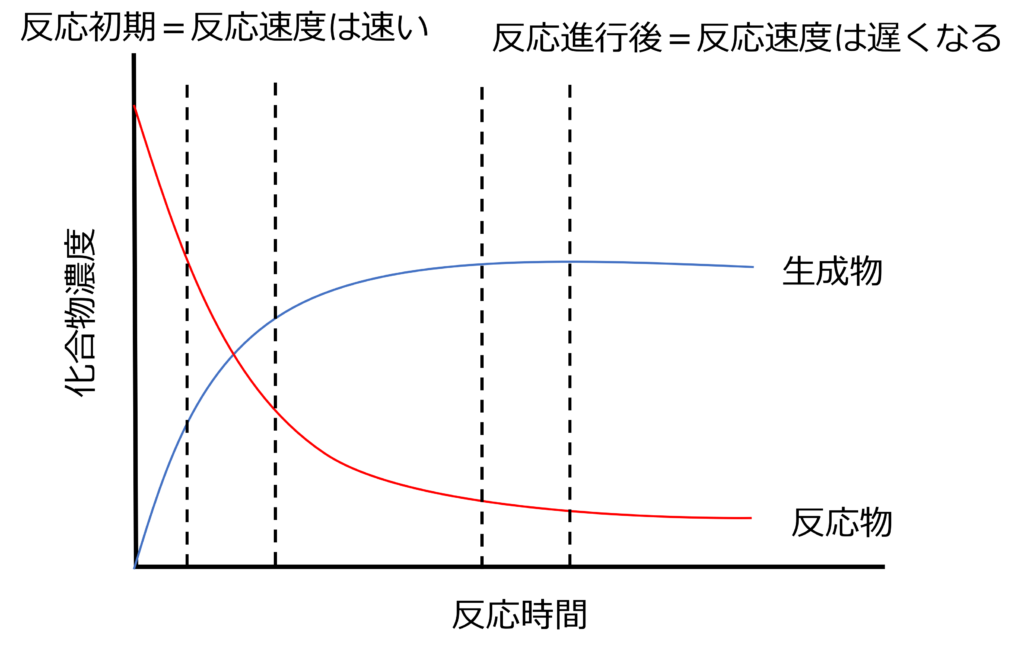
反応速度は常に一定となるわけではありません。化学反応であれば、多くの場合、時間の経過とともに反応物の濃度減少量は小さくなり、反応速度は低下することとなります。
A → Bの化学反応を考えると、反応初期はAの濃度が多いため、Aは早く減少していきます。反応が徐々に進み、Aの濃度が減少してくるとAの減少量は低下していきます。
反応初期は反応速度が速く、徐々に反応速度が減少していくため、反応のどの段階での変化量を計算するかで、反応速度は変化します。
反応速度式とは何か
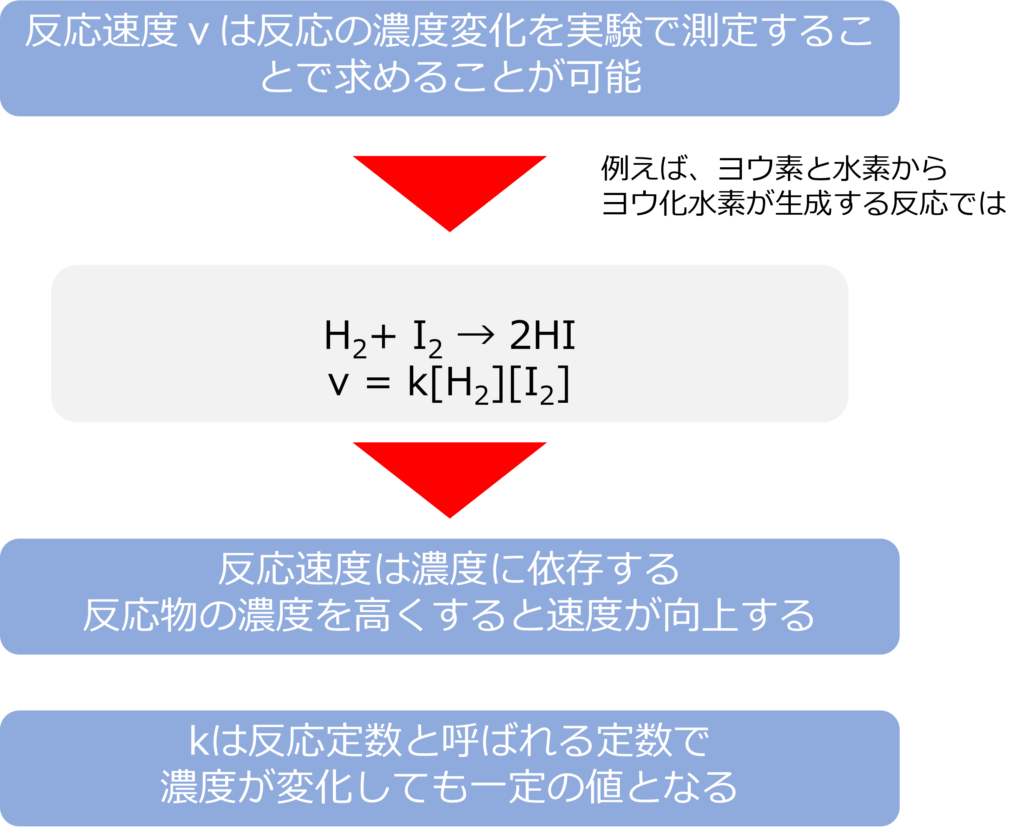
水素とヨウ素を反応させて、ヨウ化水素が生成する反応(H2+ I2 → 2HI)で、反応速度vは実験によって以下のような式でも表されることが分かっています。
v = k[H2][I2]
上記の式から、反応速度は濃度に依存することが分かります。化学反応は分子同士の衝突でおこるため、濃度が高いほど反応速度は速くなります。
そのため、反応速度はなるべく早く生成物を得たい場合は、反応物の濃度を濃くして反応速度を向上させたり、反応物が減少してきたときに、反応物を追加して濃度を高くして速度を維持することが有効となります。
kは反応速度定数と呼ばれる定数で、生成物や反応物の濃度が変化しても一定の値となります。
反応速度を上げるにはどうすれば良いのか
反応物の濃度を高く保つことで、反応速度を速いまま保つことができますが、反応そのものの速度を上げる方法として、温度を高くするという方法があります。
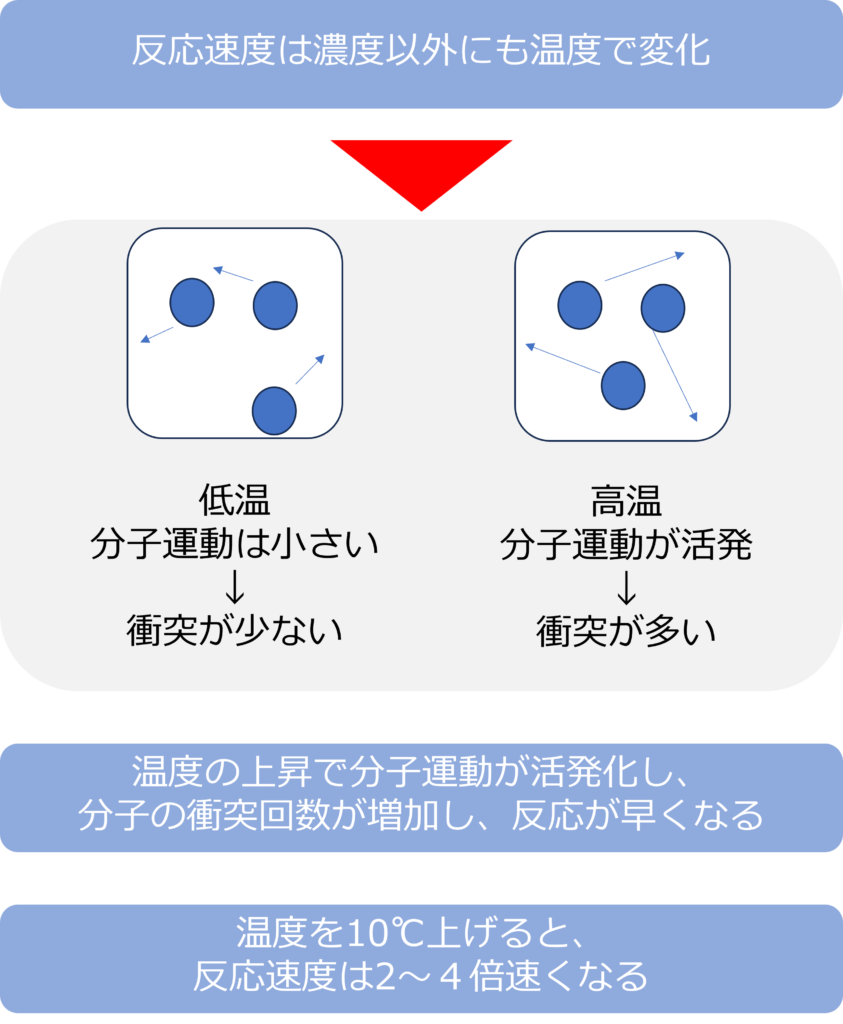
化学反応は分子同士の衝突によって、発生します。温度が高いほど、分子の運動は活発になり、衝突が発生しやすくなります。
そのため、温度の上昇は化学反応の速度を大きく上げることができます。反応の種類によっても、異なりますが、温度10℃上昇させると、反応速度は2~4倍程度速くなります、
温度以外に反応速度を上げる方法はあるのか
気体の反応であれば圧力を高くすることも、反応速度の向上に有効です。
ボイルの法則(PV =一定)から気体の圧力を高くすると、気体の体積は小さくなります。圧力をかけても、気体質量は変化しないため、反応物の濃度が上がることとなります。
圧力を大きくすることで反応物の濃度が上がるため、反応速度は上昇することなります。



コメント