この本や記事で分かること
・弱酸遊離、弱塩基遊離反応とは何か
・なぜ、弱酸や弱塩基が遊離する反応が起きるのか
弱酸、弱塩基遊離反応とは何か
弱酸と強塩基の塩と強酸を混合すると、強酸と強塩基の塩が生成し、弱酸が生成されます。このような反応を弱酸遊離反応と呼びます。
また、弱塩基と強酸の塩でも同じような現象が見られ、弱塩基が遊離します。このような反応は弱塩基遊離反応と呼ばれます。

酢酸ナトリウムと塩酸を混合すると何が起きるのか
酢酸ナトリウムは水に溶けると酢酸イオンとナトリウムイオンが生じます。
CH3COONa → CH3COO– + Na+
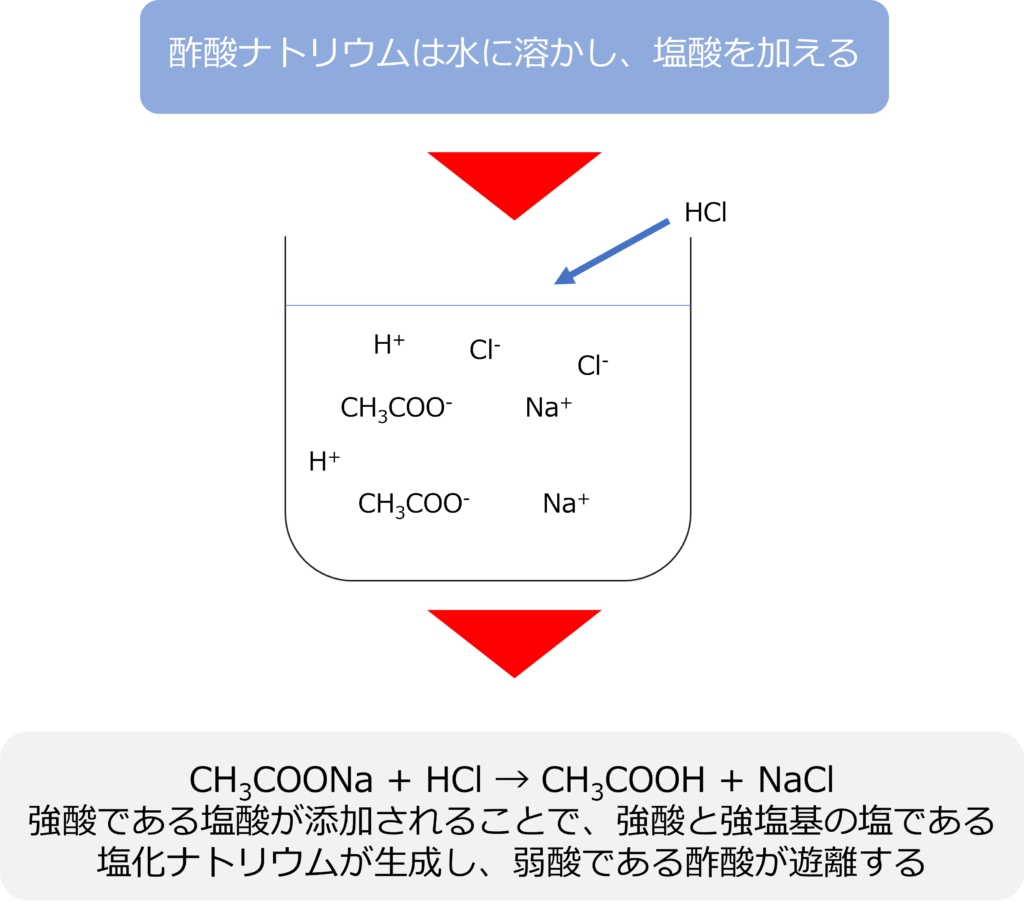
ここに塩酸を加えると、酢酸と塩化ナトリウムが生成します。
CH3COONa + HCl → CH3COOH + NaCl
酢酸ナトリウムは弱塩基である酢酸と強塩基である水酸化ナトリウムの塩であり、そこに強酸である塩酸が添加されることで、強酸と強塩基の塩である塩化ナトリウムと弱酸である酢酸が遊離します。
なぜ、弱酸である酢酸が遊離するのか
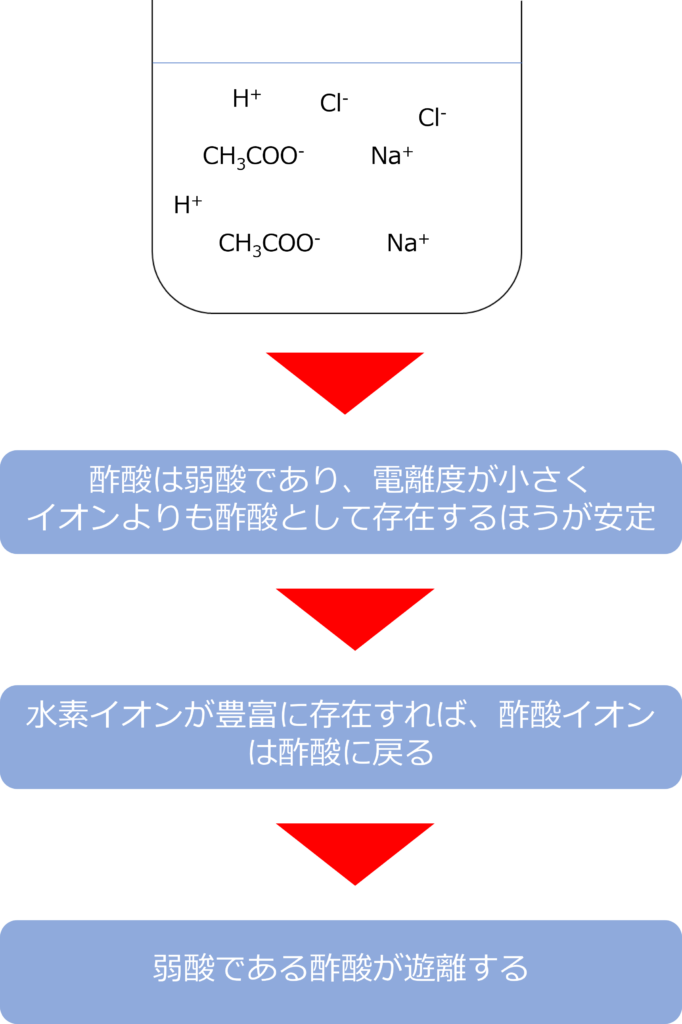
酢酸は弱酸であるため、電離度が小さく、その多くは酢酸イオンではなく酢酸として存在しています。
酢酸ナトリウム溶液には豊富な酢酸イオンが存在しており、そこに、塩酸が添加され、水素イオンが豊富になると酢酸イオンの多くは酢酸に戻るため、弱酸が遊離することとなります。
塩化アンモニウムを水に溶かすと何が起きるのか
塩化アンモニウムは弱塩基であるアンモニアと強酸である塩酸の中和によって生成する塩です。塩化アンモニウムを水に溶かすと塩化物イオンとアンモニウムイオンを生じます。
NH4Cl → NH4+ + Cl–
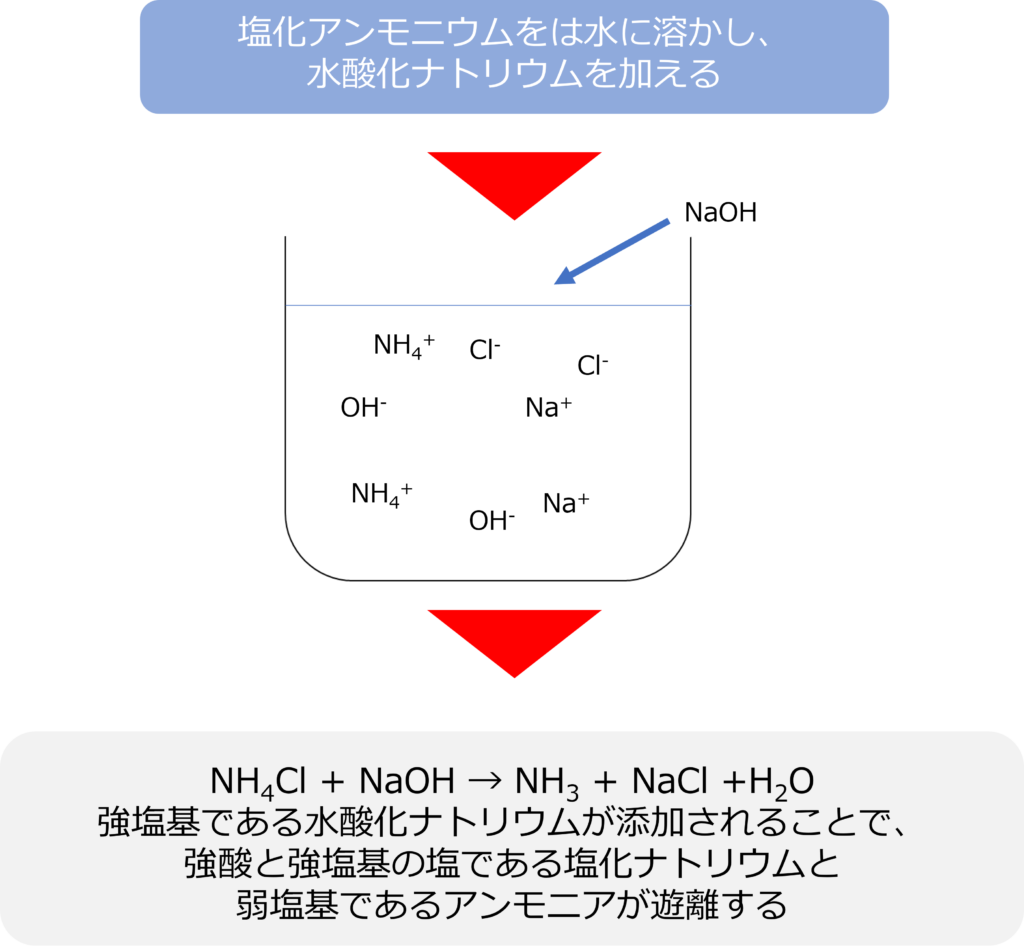
ここに強塩基である水酸化ナトリウムを加えると、弱塩基であるアンモニアと塩化ナトリウムが生じます。
NH4Cl + NaOH → NH3 + NaCl +H2O
このような反応は弱塩基遊離反応と呼ばれます。
弱塩基遊離はなぜ起きるのか
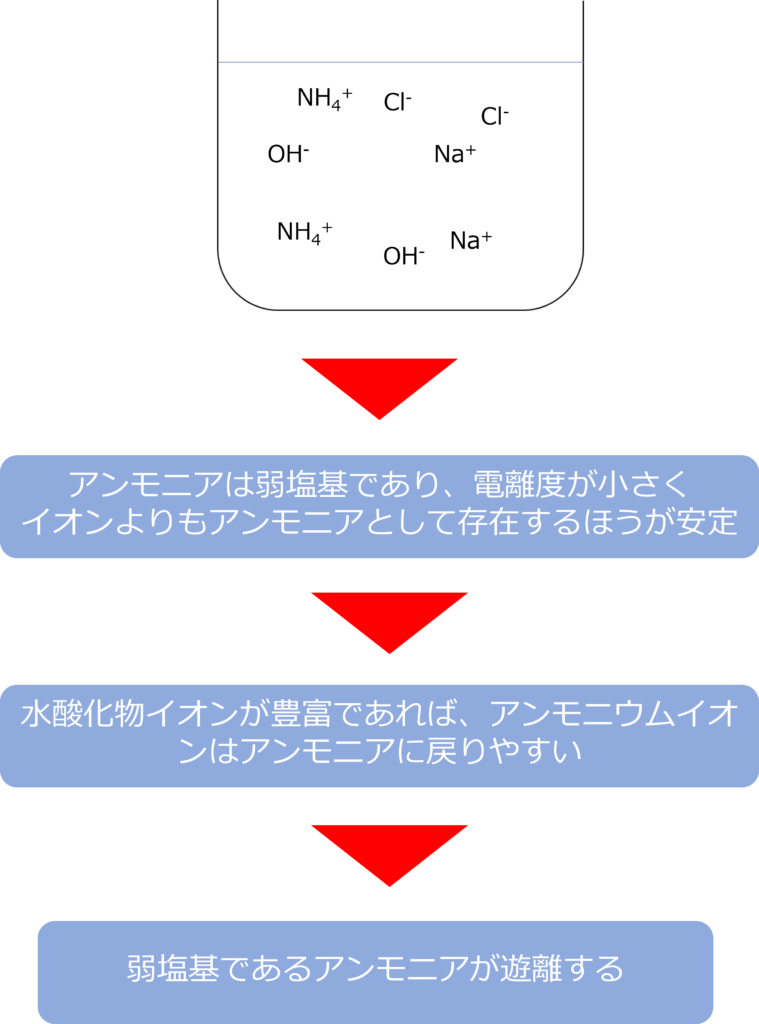
弱塩基遊離も弱酸有利と同じく、弱塩基の電離度が小さいことで発生します。強塩基によって、水酸化物イオンが豊富になると、電離度の低い弱塩基はイオンから弱塩基に戻ります。
一方で、強酸である塩化水素と強塩基である水酸化ナトリウムは電離度が高いため、イオンの状態を保ちやすく、塩として存在することになります。
このような作用で弱塩基が遊離する反応が起きています。


コメント