この記事で分かること
- UV/Vis吸光度検出器とは:液体クロマトグラフィーで使われる検出器で、紫外・可視光をフローセル内の試料に照射し、吸光度を測定して濃度を定量する方法です。芳香環などの発色団を持つ化合物に有効で、汎用性が高い特徴があります。
- なぜ芳香環などに有効なのか:π電子やn電子が紫外光のエネルギーでπ*軌道へ励起されるためです。共役が長いほどHOMO–LUMOギャップが縮まり吸収波長が長波長側へシフトする。σ電子のみの構造は励起に真空紫外域のエネルギーが必要なため、通常のUV域では吸収しません。
LCのUV/Vis吸光度検出器
機器分析とは、化学反応を用いる古典的な化学分析に対し、物質が持つ物理的・化学的性質を精密な機器で測定し、その物質の成分や構造を分析する方法の総称です。
高感度で迅速な分析が可能であり、微量な成分や複雑な混合物も精度高く分析できるため、現代の科学技術分野で広く利用されています。
今回は液体クロマトグラフィー(LC)の検出器、UV/Vis吸光度検出器に関する記事となります。
液体クロマトグラフィーの検出器にはどんなものがあるのか
液体クロマトグラフィー(HPLC)の検出器には以下のようなものがあります。
1. UV/Vis吸光度検出器(UVD)
最も広く使われる検出器です。紫外・可視光を試料に照射し、吸光度を測定します。芳香環やカルボニル基など発色団を持つ化合物に有効で、固定波長型と可変波長型があります。
2. フォトダイオードアレイ検出器(PDA / DAD)
UVDの発展型で、複数の波長を同時に検出できます。スペクトル情報が得られるため、ピークの純度確認や化合物の同定に役立ちます。
3. 蛍光検出器(FLD)
励起光を当てて蛍光を測定します。UVDより高感度(10〜1000倍)で選択性も高く、アミノ酸・ビタミン・多環芳香族炭化水素などの微量分析に使われます。
4. 示差屈折率検出器(RID)
移動相と試料の屈折率の差を測定します。糖類・高分子・脂質など発色団を持たない化合物にも使えますが、感度は低く、グラジエント溶出には不向きです。
5. 電気化学検出器(ECD)
酸化還元反応を利用して電流を測定します。カテコールアミン・フェノール類など電気化学活性な化合物に非常に高感度です。
6. 質量分析検出器(MS / LC-MS)
イオン化した分子の質量を測定します。高感度・高選択性で構造情報も得られるため、医薬品・環境分析・プロテオミクスなど幅広い分野で活躍します。タンデム型(MS/MS)はさらに高い選択性を持ちます。
7. 蒸発光散乱検出器(ELSD)
移動相を蒸発させ、残った粒子にレーザーを当てて散乱光を検出します。脂質・糖類・界面活性剤など揮発しない化合物全般に使えます。
8. 荷電粒子検出器(CAD)
ELSDと似た原理ですが、粒子を帯電させて電流を測定します。ELSDより再現性・感度が高いとされています。
9. 電気伝導度検出器
イオンクロマトグラフィーで主に使われ、イオン性化合物(陰イオン・陽イオン)の検出に特化しています。
UV/Vis吸光度検出器とは何か
UV/Vis吸光度検出器(UVD)は、紫外・可視光を試料に照射し、吸光度を測定します。
基本原理
ランベルト・ベールの法則に基づいています。
吸光度 A = ε × c × l
- ε:モル吸光係数(化合物固有の値)
- c:濃度
- l:光路長
光源から出た光が試料セル(フローセル)を通過する際、化合物が特定の波長の光を吸収します。その吸収量(吸光度)を測定することで濃度を定量します。
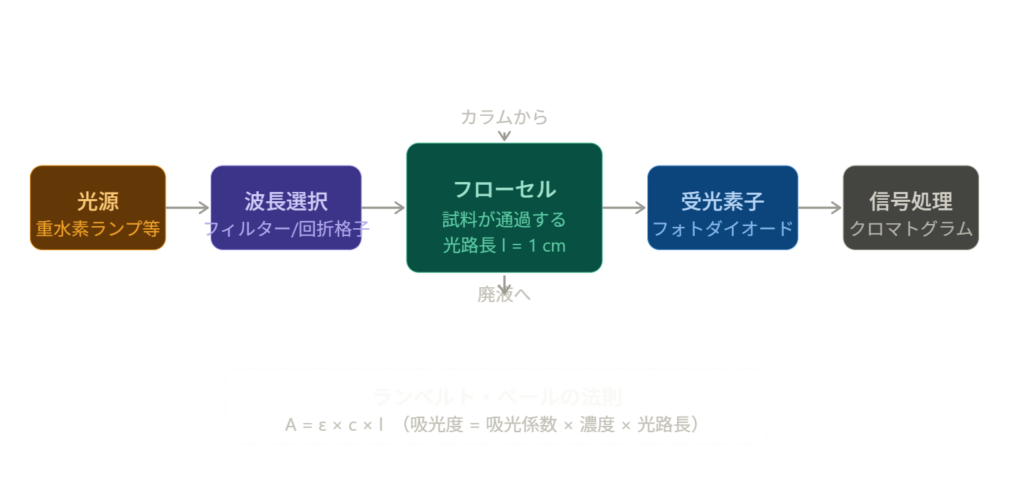
光源(重水素ランプや タングステンランプ)から出た光が、波長選択部(フィルターや回折格子)で特定の波長に絞られます。
その後、カラムから流れてきた試料が通過するフローセルを照射し、受光素子(フォトダイオー ド)が透過光の強さを測定します。
試料がないとき(基準)と比べて透過光が弱くなった割合を吸光度として計算し、クロマトグラムを出力します。
特徴
- 感度の目安:一般的に ng〜μg レベルの検出が可能です。
- 対象化合物:紫外光を吸収する発色団(芳香環・カルボニル基・共役二重結合など)を持つ化合物が対象です。逆に、糖類・脂肪酸など発色団を持たない化合物には感度が低いのが弱点です。
- 測定波長:よく使われるのは 254 nm(芳香族化合物)や 280 nm(タンパク質・アミノ酸)などです。化合物の最大吸収波長(λmax)に合わせると感度が最大になります。
- グラジエント溶出との相性:移動相の組成変化が吸光度に影響することがあるため、使用する溶媒の UV カットオフ波長(透明な波長範囲)を確認する必要があります。

液体クロマトグラフィーで使われる検出器で、紫外・可視光をフローセル内の試料に照射し、吸光度(ランベルト・ベールの法則)を測定することで濃度を定量します。芳香環などの発色団を持つ化合物に有効で、汎用性が高い。
ランベルト・ベールの法則とは何か
もともとは2つの独立した法則が合わさったものです。
- ランベルトの法則(1760年):光の吸収量は光路長に比例する
- ベールの法則(1852年):光の吸収量は濃度に比例する
この2つを組み合わせたのがランベルト・ベールの法則です。
法則の詳細
吸光度 A は入射光 I₀ と透過光 I の比の対数で定義されます。
A = log₁₀(I₀ / I)
この A がちょうど ε × c × l に等しくなる、というのがこの法則の核心です。吸光度が 1 のとき透過率は 10%、2 のとき 1% になります。
成立する条件(限界)
法則が成立しない場合もあり、注意が必要です。
高濃度(一般に 0.01 mol/L 以上)になると分子間の相互作用が生じ、比例関係が崩れます。また、測定に用いる光が単色でなく広い波長帯を持つ場合も偏差が生じます。さらに、散乱粒子を含む懸濁液や蛍光を発する試料では正確な測定が困難です。
分析への応用
未知試料の濃度を求めるときは、既知濃度の標準溶液で検量線(A vs c のグラフ)を作成し、そこに試料の吸光度を当てはめて逆算します。これが UV/Vis 検出器における定量分析の基本的な流れです。

ランベルト・ベールの法則とは、光が物質を通過するときの吸収量を表す法則です。
A = ε × c × l
- A:吸光度(absorptance)
- ε:モル吸光係数(物質固有の光の吸収しやすさ)
- c:濃度(mol/L)
- l:光路長(cm)
つまり、「濃度が高いほど」「光路長が長いほど」吸光度は大きくなる、という比例関係を示しています。これにより吸光度を測れば濃度を逆算できるため、定量分析の基礎となっています。
芳香環・カルボニル基などはなぜ紫外光を吸収するのか
芳香環・カルボニル基・共役二重結合は紫外光を吸収するのは、π電子が紫外光のエネルギーとちょうど共鳴するためです。
電子遷移の基本
分子が光を吸収するのは、光子のエネルギーが電子を低いエネルギー準位から高い準位へ跳び上がらせる(励起する)ときだけです。このエネルギーが紫外域(200〜400 nm)に対応するのが、π電子系の遷移です。### π軌道とは何か
炭素の二重結合(C=C)では、σ結合(軸方向)のほかに、p軌道が横向きに重なったπ結合が生まれます。このπ電子は σ電子より弱く束縛されており、励起に必要なエネルギーが小さくなります。その結果、遠紫外〜近紫外領域の光(数eV相当)でちょうど励起できます。
共役によるギャップの縮小
単独の二重結合(C=C)だけなら吸収波長は 185 nm 付近(遠紫外域)で、通常のHPLC測定では観測しにくい領域です。
しかし二重結合が交互につながる共役系になると、π電子が分子全体に非局在化し、軌道のエネルギー差(HOMO–LUMOギャップ)が縮まります。
共役が長くなるほど吸収波長は長波長側へシフトし、200〜400 nm の測定しやすい紫外域に入ってきます。ベンゼン環(芳香環)はこの共役が環状に閉じた特別な安定構造で、254 nm 付近に強い吸収を持ちます。
カルボニル基の特殊性:n→π* 遷移
カルボニル基(C=O)では、酸素の孤立電子対(n軌道)が関わる別の遷移も起こります。n→π* 遷移と呼ばれ、280〜330 nm 付近に現れます。π→π* 遷移より吸光係数(ε)が小さく、吸収は弱いものの、より長波長側にあるため測定には有利な場合があります。
まとめ
| 構造 | 遷移の種類 | 吸収波長の目安 |
|---|---|---|
| 単純 C=C | π→π* | ~185 nm(遠紫外) |
| 共役ジエン | π→π* | ~250 nm |
| ベンゼン環 | π→π* | ~254 nm |
| カルボニル(C=O) | n→π* | ~280 nm |
| 長い共役系 | π→π* | 400 nm 以上も |
σ電子や孤立した単結合は励起に必要なエネルギーが非常に大きく、真空紫外域(< 180 nm)にしか吸収がないため、通常の UV/Vis 検出器では検出できません。これが「発色団を持たない化合物はUVで検出しにくい」理由です。

π電子やn電子(孤立電子対)は束縛が弱く、紫外光のエネルギーでπ*軌道へ励起されます。共役が長いほどHOMO–LUMOギャップが縮まり、より長波長の光を吸収します。σ電子のみの構造は励起に高エネルギーが必要なため紫外域では吸収しません。


コメント